СЕМИОТИКА НАРУШЕНИЙ ВОДНО-ЭЛЕКТРОЛИТНОГО ОБМЕНА Все жизненно важные химические и физические процессы, особенно ферментативные, нормальная терморегуляция в организме ребенка происходят в системах жидкостей. Количество, состав и химические реакции этих «телесных соков» поразительно постоянны, хотя нагрузки со стороны внешнего мира изменяются. Согласно классическому определению физиолога Клода Бернара, именно это постоянство является «основным условием самостоятельной, независимой жизни». У здорового человека . поддерживается равенство объемов выделяющейся из организма и поступившей в него за сутки воды, что называется водным балансом организма. В этом контексте можно рассматривать также и баланс электролитов: натрия, калия, кальция и др. Средние показатели водного баланса здорового человека в состоянии покоя представлены в табл. Содержание общего количества воды (в процентах) и соотношение в распределении жидкости в зависимости от возраста
Содержание воды в разных тканях варьирует от 20 % в жировой ткани до 83—90 % в почках и крови, у девочек и женщин в связи с большим количеством жировой клетчатки содержание воды ниже, чем у мальчиков и мужчин. Ткани и органы детского организма содержат большее количество воды, чем взрослого человека. У новорожденного на долю воды приходится около 80% от массы тела. Наиболее интенсивно он теряет жидкость в первые дни жизни — происходит физиологическая убыль массы тела (5—7 %) преимущественно путем испарения ее при дыхании и с поверхности кожи, а также экскреции воды с мочой и калом. У детей в возрасте до 5 лет содержание воды в организме составляет около 70 % от массы тела. Количество жидкости в организме ребенка зависит, кроме того, от характера питания и содержания жира в тканях. При углеводистом питании гидрофильность тканей увеличивается. Жировая ткань, напротив, бедна водой (около 22%), и при ожирении ее количество в организме уменьшается. Повышение потребления белков и, соответственно, конечное превращение их в мочевину, удаляемую из организма с мочой, ведет к абсолютной необходимости возрастания потерь воды в почках, что требует повышенного ее поступления в организм. Напротив, при питании преимущественно пищей, богатой углеводами и жиром, и небольшом поступлении в организм поваренной соли потребность организма в поступлении воды меньше. Хотя общее количество жидкости на 1 кг массы тела у детей больше, чем у взрослых, на 1 м2 поверхности тела содержание жидкости у детей значительно меньше. Водный обмен у детей протекает более интенсивно, чем у взрослых, у которых вся вода в организме обновляется примерно каждый месяц, а внеклеточное водное пространство — каждую неделю. У грудного ребенка время пребывания молекулы воды в организме составляет 3—5 дн. В отличие от взрослых у детей раннего возраста отмечается большая проницаемость клеточных мембран, а фиксация жидкости в клетке и межклеточных структурах более слабая. Особенно это касается межуточной ткани, так как кислые му-кополисахариды основного вещества определяют прочность этой связи. Величину отдельных пространств, занимаемых жидкостью, можно определить с помощью методов разведения с применением таких веществ, которые распределяются равномерно или во всех жидкостях организма, или только во внеклеточной жидкости (хлоридное пространство), или только в плазме крови, либо можно определить лабильную, не связанную с кислыми мукополисахаридами воду (инулиновое пространство). У ребенка объемы хлоридного и инулинового пространств почти одинаковы: 41,2 и 40 % от массы тела, у взрослого же они соответственно равны 26,4 и 16 %, что свидетельствует о большей лабильности водного обмена у детей. С помощью изотопов можно определить общее содержание натрия, калия и хлора в организме. Хотя жидкости организма представляют собой единое целое, химический состав их различен. Принято различать внеклеточную и внутриклеточную жидкости, разделенные мембранами. При патологии появляется третье водное пространство — вода полостей тела: брюшной, плевральной и т. д. Объем внеклеточной жидкости составляет 20—25 % от массы тела и состоит из жидкой части плазмы (5 % от массы тела), интерстициальной жидкости (15 % от массы тела) и трансцел-люлярной жидкости (1—3 % от массы тела), которая состоит из секретов желудочно-кишечного тракта и спинномозговой, внутриглазной, плевральной, перитонеальной и синовиальной жидкостей. Объем трансцеллюлярной жидкости значительно увеличивается при воспалительных заболеваниях кишечника (диарее, кишечной непроходимости, плеврите и др.). Плазма крови отделяется капиллярной стенкой от межклеточной (интерстициальной) жидкости, а последняя отделяется клеточной мембраной от внутриклеточной (интрацеллюлярной) жидкости. Благодаря сходному химическому составу плазма и интерстициальная жидкость составляют функциональное единство — экстрацеллюлярную (внеклеточную) жидкость. Межклеточная жидкость подразделяется на мобильную, свободную часть ультрафильтрата плазмы, располагающуюся между клетками и капиллярами, и менее мобильную, находящуюся в соединительной ткани. Уменьшение с возрастом содержания внеклеточной жидкости в основном обусловлено увеличением роста клеток и уменьшением скорости роста коллагена по отношению к мышечной ткани. Экстрацеллюлярная жидкость является той внутренней средой, в которой живут клетки, следовательно, она обеспечивает оптимальные условия для их жизнедеятельности. Плазма крови образует большую транспортирующую систему, которая питает клетки и уносит продукты обмена веществ. Только экстрацеллюлярная жидкость связана с внешней средой через желудочно-кишечный тракт, легкие, кожу и почки. Жизненно важной функцией этой жидкости является поддержание нормального количества плазмы крови и тем самым — обеспечение кровообращения. При потере воды вода из этого резерва направляется в плазму, при избытке — из плазмы отводится в это пространство. Накопление или потеря электролитов также отражаются на ионном соотношении как плазмы, так и всей экстра-целлюлярной жидкости. Объем внутриклеточной жидкости составляет в среднем около 40 % от массы тела. Она представляет собой сумму жидкостей в клетках, имеющих разные локализацию, функцию, состав. Известно, что вода и соль никогда не циркулируют одна без другой. Состав минеральных солей и их концентрация определяют осмотическое давление жидкостей, которое является, по мнению И.М. Воронцова, наряду с макро- и микроскопической анатомией так называемой ионной анатомией. Важнейшие катионы: натрий, калий (одновалентные); кальций, магний (двухвалентные). Им соответствуют анионы хлора, карбоната, ортофосфата, сульфата и др. Концентрации катионов и анионов уравновешены таким образом, что реакция несколько сдвинута в щелочную сторону (рН 7,35—7,45), то есть имеется некоторый избыток оснований. Предложено выражать концентрацию электролитов графически в виде ионограммы.
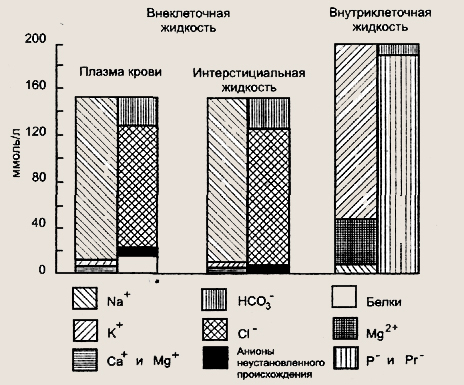
Электролитный состав внеклеточной и внутриклеточной жидкостей в организме Как видно из рисунка, основным различием в структуре электролитов в этих двух больших системах жидкостей является то, что в клетках содержатся в основном калий, фосфаты и белок; ионы хлора в большинстве клеток почти полностью отсутствуют, концентрация натрия низка, в то время как экстрацеллю-лярная жидкость содержит в основном натрий, ионы хлора и бикарбоната. Практически плазма крови и межклеточная жидкость являются растворами натрия, хлора, бикарбоната; там присутствуют, хотя и в незначительных количествах, жизненно важные ионы калия, кальция, магния, фосфора; кроме того, в плазме содержится 6—8 % белка. Такое распределение ионов в экстра- и интрацеллюлярной системах представляет собой динамическое равновесие: из экстрацеллюлярной жидкости, где концентрация натрия высока, он постоянно поступает в клетки, однако энергия, выделяющаяся при метаболических процессах, «высасывает» из клеток столько же натрия, сколько его проникает туда. Нарушение нормальной жизнедеятельности клетки парализует натриевый насос: калий выходит из клеток, и натрий занимает его место, то есть водный баланс организма тесно связан с обменом электролитов. Суммарная концентрация минеральных и других ионов создает определенную величину осмотического давления. Концентрация отдельных минеральных ионов определяет функциональное состояние возбудимых и невозбудимых тканей, а также состояние проницаемости биологических мембран. Поскольку синтез минеральных ионов в организме не осуществляется, они должны поступать в организм с пищей и питьем. Данные о физиологической роли и пищевых источниках минеральных ионов приведены в таблице. Микрокомпоненты пищи (минеральные вещества)
Для обеспечения физиологических процессов важна не столько общая концентрация каждого из электролитов в водных пространствах, сколько их активность или эффективная концентрация свободных ионов, поскольку часть ионов находится в связанном состоянии (кальций и магний — с протеинами, натрий — в ячейках клеточных органелл и т. п.). Роль отдельных электролитов в жизнедеятельности организма многообразна и неоднозначна. Физиологическая роль основных ионов. Натрий (Na). В организме взрослого человека содержится 70—100 г натрия, у детей его содержание ниже. Он обнаруживается во всех тканях, главным образом в виде катионов натрия. Содержание натрия в плазме крови 130—150 ммоль/л. Натрий — главный внеклеточный катион: на его долю приходится более 90 % всех катионов плазмы. Около 85 % ионов натрия представлено в свободной форме и приблизительно 15 % его удерживается белками. Во внеклеточных жидкостях находится около 40 % всего натрия, около 50 % — в костях и хрящах и менее 10 % — внутри клеток. Натрий создает и поддерживает осмотическое давление жидкостей организма (преимущественно внеклеточной), задерживает воду в организме, участвует во всасывании в кишечнике и реабсорбции в почках глюкозы и аминокислот. Натрий участвует в регуляции кислотно-щелочного состояния организма, является щелочным резервом крови, активатором некоторых ферментов. Содержание натрия в клеточной микросреде определяет величину мембранного потенциала и, соответственно, возбудимость клеток. Совместно с ионами калия натрий стимулирует АТФазную активность фракций клеточных мембран, стабилизирует симпатический отдел нервной системы, принимает участие в регуляции тонуса сосудов. Основное количество натрия поступает в организм с поваренной солью, небольшое количество его ребенок потребляет в виде бикарбоната натрия, цитрата, сульфата и глутамата натрия, которые как добавки встречаются в продуктах питания. Суточная потребность ребенка в натрии составляет в среднем 1,5—2,0 ммоль/л. Около 95 % поступившего натрия всасывается в желудочно-кишечном тракте с помощью blа+глюкоза (blами-нокислота) и Naycr-котранспортной системы кишечника (тонкого и толстого), электрогенного всасывания. Основное количество натрия (около 95 %) выводится почками с мочой в виде натриевых солей фосфорной, серной, угольной и других кислот. Натрий выводится также с потом и через кишечник. Дефицит или избыток натрия вызывают серьезные изменения в организме ребенка (см. Семиотика нарушений обмена некоторых ионов). Калий (К+) в отличие от натрия является внутриклеточным катионом. У взрослых содержание калия составляет приблизительно 53 ммоль/кт и 95 % его обменивается. Уровень калия в организме ребенка ниже. Основное количество калия (90 %) находится внутри клеток в виде непрочных соединений с белками, углеводами и фосфором и менее 10 % — внеклеточно. Часть калия содержится в клетках в ионизированном виде и обеспечивает мембранный потенциал. В плазме и межклеточной жидкости находится 2—5 % общего калия. Во внеклеточной среде небольшое количество калия находится преимущественно в ионизированном виде. Наиболее богата калием мышечная ткань. В эритроцитах калия в 15—20 раз больше, чем в плазме, в которой содержится 4—5 ммоль/л калия. Суточная потребность взрослого человека в калии 2—3 г, ребенка — 1,5—2,0 ммоль/л. Основным пищевым источником калия являются продукты растительного происхождения. Из организма калий выводится преимущественно почками (80—90 %), в меньшей степени пищеварительным трактом и потовыми железами. Основным регулятором выведения его с мочой является альдостерон. Калий участвует в ряде жизненно важных физиологических процессов: вместе с натрием создает и поддерживает осмотическое давление жидкостей организма (преимущественно внутриклеточной), участвует в регуляции кислотно-щелочного состояния организма. Калий — активатор ряда ферментов, вместе с Na+ генерирует электрохимический потенциал в мембранах клеток. Уровень калия в клетках и внеклеточной среде играет важнейшую роль в деятельности сердечно-сосудистой, мышечной и нервной систем, в секреторной и моторной функциях пищеварительного тракта, экскреторной функции почек. Обычно выход калия из клеток зависит от увеличения их биологической активности, распада белка и гликогена, недостатка кислорода. Концентрация калия увеличивается при ацидозе и снижается при алкалозе. Дефицит и избыток калия вызывают серьезные изменения в организме ребенка. Кальций (Са2+) в различных тканях содержится внутрикле-точно и почти исключительно в форме растворимых белковых комплексов. Лишь в костной ткани, включающей до 97 % всех запасов кальция в организме, он находится главным образом в виде нерастворимых внеклеточных включений гидроксиапатита. Содержание кальция в организме у детей составляет около 200 ммоль/л, у взрослых — 475 ммоль/л. В крови кальций содержится в форменных элементах и плазме. Содержание кальция в крови поддерживается в норме в диапазоне 2,5—2,8 ммоль/л. Приблизительно 40 % его связано с белком (из них на связь с альбумином приходится 80—90 %), остальные 60 % кальция фильтруются или диффундируют (из них около 14 % связано с анионами, такими как фосфат или цитрат, оставшиеся 46 % (1,2 ммоль/л) присутствуют в виде свободных ионов). Основной источник кальция — продукты питания: молоко и молочные продукты, яйца, бобовые, сухофрукты и др. Для детей грудного возраста основной источник кальция — молоко. У взрослого человека поддерживается нулевой баланс кальция, у детей — положительный. Ежесуточная экскреция через почки составляет 100—200 мг, через кишечник — 150 мг, небольшое количество (до 20 мг) выводится с потом. Потери кальция с мочой увеличиваются при ацидозе и потреблении больших количеств белка. Кальций участвует в физиологических процессах только в ионизированном виде. Кальций — необходимый участник процесса мышечного сокращения, важнейший компонент свертывающей системы крови (превращения протромбина в тромбин, фибриногена в фибрин, способствует агрегации тромбоцитов), как кофактор или активатор участвует в работе многих ферментов. Он входит в состав костей и хрящей в форме апатитов, является стабилизатором клеточных мембран, регулирует возбудимость нервов и мышц. Кальций — внутриклеточный посредник в действии некоторых гормонов на клетку, универсальный триггер многих секреторных процессов (секреция гормонов, гиста-мина из гранул тканевых базофилов, тучных клеток, выделение медиаторов при синаптической передаче возбуждения). Ионизация кальция зависит от рН крови. При ацидозе содержание ионизированного кальция повышается, а при алкалозе падает. Алкалоз и снижение уровня кальция ведут к резкому повышению нейромышечной возбудимости и тетании. Магний (Mg2+), как и калий, является основным внутриклеточным катионом, так как его концентрация в клетках значительно выше, чем во внеклеточной среде. Общее количество магния в организме у детей составляет 11 ммоль/л, у взрослых — 14 ммоль/л. Половина всего магния находится в костях (1/3 этого количества свободно обменивается), 49 % — в клетках мягких тканей, он играет существенную роль во многих ферментативных реакциях, в том числе в активации АТФ-азы. Более 50 % всего внутриклеточно локализованного магния находится в мышцах и большая часть в печени. Только 20—30 % магния, входящего в клетки, обменивается, остальное количество связано с белками, РНК и АТФ. Лишь 1 % магния находится во внеклеточном водном пространстве. Уровень магния в крови составляет 0,75—0,9 ммоль/л, при этом более 60 % катиона находится в ионизированном виде. Суточная потребность в магнии взрослого человека составляет около 300 мг. Овощи с зелеными листьями и фрукты, бобовые и злаки, мясо являются основными пищевыми источниками магния. Значительное количество эндогенного магния поступает в пищеварительный тракт с пищеварительными секретами. Главным регулятором содержания магния в организме являются почки. При недостатке его в организме он полностью реабсорбируется почками. Через желудочно-кишечный тракт с пищеварительными секретами происходит удаление из организма избытка магния. Магний — структурный элемент костной ткани. Он стабилизирует биологические мембраны, уменьшая их текучесть и проницаемость. Образуя хеаты с нуклеиновыми кислотами, он стабилизирует структуры ДНК, ассоциации субъединиц рибосом, связанные транспортными РНК с рибосомой. Магний образует малостабильный комплекс с АТФ (М§2+-АТФ) и облегчает гидролиз АТФ. Магний входит в состав более 300 разных ферментных комплексов, обеспечивая их активность. Катион Mg2+ уменьшает возбудимость нервно-мышечной системы, сократительную способность миокарда и гладких мышц сосудов, оказывает деп--рессивное действие на психические функции. При дефиците магния повышается возбудимость ЦНС, что проявляется слабостью и расстройством психики (спутанность сознания, беспокойство и агрессивность), возникновением судорог. Повышение уровня магния в плазме (более 1,5 ммоль/л) вызывает тошноту и рвоту. Высокие концентрации магния могут вызвать гипотензию. Главным анионом внеклеточной жидкости является хлор (С1+), в организме он находится преимущественно в ионизированном состоянии в форме солей натрия, калия, кальция, магния и т. д. Общее количество его в организме составляет 33 ммоль/кг. Распределение хлоридов в жидкостях организма определяется распределением ионов натрия. В крови хлориды встречаются главным образом в виде натрия хлорида. Концентрация хлора в плазме крови в норме колеблется от 90 до 105 ммоль/л. 90 % аниона хлора находится во внеклеточной жидкости. Суточная потребность (2—4 г) полностью покрывается поваренной солью, добавляемой в пищу. Хлориды участвуют в создании и поддержании осмотического давления жидкостей организма, в синтезе соляной кислоты (НС1) в желудке. Хлориды также участвуют в генерации электрохимического градиента на плазматических мембранах клеток, являются активаторами ряда ферментов. Согласно большинству клинических наблюдений, изменение концентрации хлора в крови происходит соответственно изменению концентрации натрия. Однако иногда изменение концентрации хлора не сопровождается эквивалентными изменениями концентрации натрия. Избыток хлора ведет к ацидозу. Измерение в сыворотке уровня хлорида необходимо для определения у больного анионной щели. В норме уровень сывороточного катиона натрия больше суммы концентраций двух наиболее распространенных анионов сыворотки — хлора и гидрокарбоната. Разность между ними — анионная щель — в норме составляет 8—12 ммоль/л. Она образуется из общей концентрации неизмеряемых анионов, таких как фосфат, сульфат, белки и органические кислоты, превышающей концентрацию неизмеряемых катионов, в основном кальция, калия и магния. Измерение анионной щели позволяет определить изменение концентрации неизмеряемых анионов и катионов. Фосфор (Р) имеет исключительно большое биологическое значение для растущего организма. Около 70 % его сосредоточено в костной ткани, он входит в состав межклеточной жидкости и активных биохимических соединений каждой клетки организма. Фосфаты являются основными анионами внутриклеточной жидкости, где концентрация их выше, чем во внеклеточной среде, в 40 раз. Содержание неорганического фосфора в крови составляет 0,94— 1,60 ммоль/л, у детей первого года жизни — 1,26— 2,26 ммоль/л. Потребность в фосфатах взрослого человека — около 1200 мг/сут. Фосфор в достаточном количестве присутствует в пищевом рационе, так как содержится практически во всех пищевых продуктах и всасывается (около 50 %) в виде неорганических фосфатов. Экскреция осуществляется почками и через кишечник. Паратгормон усиливает экскрецию фосфатов с мочой. Экскреция возрастает и при увеличении уровня неорганического фосфора в плазме крови. Фосфаты — необходимый компонент клеточных мембран, играют ключевую роль в метаболических процессах, входя в состав многих коферментов, нуклеиновых кислот и фосфопротеи-дов. Фосфат — структурный компонент костей и зубов в виде апатитов, участвует в регуляции концентрации водородных ионов (фосфатная буферная система), важнейший компонент фосфор-органических соединений организма: нуклеотидов, нуклеиновых кислот и фосфопротеидов, фосфолипидов, фосфорных эфиров углеводов, коферментов, 3-ФКГ и др. Органические соединения фосфора — АТФ, АДФ — составляют основу энергетического обмена. Избыток фосфора в организме встречается редко и наблюдается при нарушении функции почек или гипофункции паращи-товидных желез. Это приводит к гипокальциемии и нарушению метаболизма костной ткани. Проявлениями недостатка фосфора являются ломкость костей, нарушение диссоциации оксиге-моглобина, слабость, миопатия, кардиомиопатия. Сульфаты в большем количестве содержатся во внутриклеточном пространстве, входят в состав многих биологически активных веществ. В плазме крови неорганических сульфатов содержится 0,3—1,5 ммоль/л. Они необходимы для обезвреживания токсических соединений в печени. Бикарбонат. Ион бикарбоната (НСО'.,) в наибольшем количестве содержится в экстрацеллюлярной жидкости. Он находится в динамическом равновесии с угольной кислотой (20:1) и является компонентом основной буферной системы организма. Средняя концентрация бикарбоната в сыворотке крови — 27 мэкв/л. Величина концентрации бикарбоната у недоношенных новорожденных колеблется в пределах 11—29 ммоль/л (средняя 20), у доношенных новорожденных — 21 ммоль/л (16—25). Водно-солевой обмен. Водно-солевым обменом называется совокупность процессов поступления воды и электролитов в организм, распределения их во внутренней среде и выделения из организма. Жидкости организма не застаиваются в анатомических пространствах, в них постоянно протекают интенсивные процессы внутреннего обращения: фильтрационные, секреторные, диффузионные и осмотические. Гидростатическое давление крови вытесняет из артериальных капилляров жидкость, которая через лимфатические пути и венозные капилляры попадает вновь в венозную систему. При различных возмущающих воздействиях (температурные сдвиги среды, разный уровень физической активности, изменение характера питания) отдельные показатели баланса могут меняться. При участии воды формируются такие структуры, как клеточные мембраны, транспортные частицы крови, макромолекулярные и надмолекулярные образования. В процессе обмена веществ и окисления водорода, отделенного от субстрата, образуется эндогенная «вода окисления», причем ее количество зависит от вида распадающихся субстратов и уровня обмена веществ. Водно-электролитный обмен у детей чрезвычайно лабилен. У них очень легко возникают состояния как гипер-, так и дегидратации. При этом одновременно может изменяться и осмоляр-ность жидкостей, что клинически проявляется различными синдромами. Постоянство состава жидкостей связано с поступлением их в организм с пищей и выведением из организма. Осмоляр-ность плазмы почти постоянна и сохраняется на уровне 285— 295 мосм/л, независимо от постоянного колебания количества потребляемых растворов и воды. Нужно учитывать также воду, образующуюся в организме в результате обмена веществ, — ок-сидазную. Так, в покое при окислении 100 г жира образуется более 100 мл воды, 100 г белка — около 40 мл воды, 100 г углеводов — 55 мл воды. Допустимо образование воды в организме ребенка в количестве 12 мл/кг массы тела. Повышение катаболизма и энергетического обмена ведет к резкому увеличению образуемой эндогенной воды. Однако эндогенной воды у человека недостаточно для обеспечения водной среды метаболических процессов, особенно выведения в растворенном виде продуктов метаболизма. Важно помнить, что вода входит в состав различных органических систем, например каждый грамм гликогена содержит 1,5 мл воды, а каждый грамм белка — 3 мл воды. Вода и электролиты выводятся из организма тремя основными путями: с мочой, с калом, путем испарения через легкие и кожу (perspiratio insensibilis). Потери жидкости через кожу и легкие вместе с частью мочи, необходимой для выведения растворенных в ней веществ, составляют обязательные потери. Они представляют собой минимальный объем жидкости, который должен потреблять человек для поддержания водного баланса. У маленьких детей выведение воды путем perspiratio insensibilis составляет до 50—75 % от общей величины. Интенсивность экстраренальной потери воды у детей в 2 раза выше, чем у взрослых, и составляет в среднем 1 мл/кг массы тела в час, у взрослых -0,45 мл/кг в час. Общие потери воды путем перспирации у взрослых составляют 14 мл/кг в сутки, у детей — до 45 мл/кг (15 мл/кг через легкие, 30 мл/кг через кожу). Через кишечник ребенок теряет 40—80 мл, через почки — 90—100 мл воды на 1 кг массы тела. Это объясняется относительной незрелостью почек и относительно большой поверхностью тела. Потери за счет испарения регулируются факторами, в целом не зависящими от содержания воды в организме. Они пропорциональны площади поверхности тела и зависят от температуры как тела, так и окружающей среды, частоты дыхания и парциального давления водяных паров в воздухе. Потоотделение незначительно при температуре окружающего воздуха 26,5—29,5 °С, начиная с 30,5 °С оно возрастает на 30 мл/100 ккал с каждым градусом, однако эти расчеты неприемлемы у недоношенных детей, которым необходима более высокая температура окружающей среды. Потоотделение частично контролируется вегетативной нервной системой. Оно может быть снижено при тепловых стрессах, тяжелых дефицитах жидкостей организма или увеличении концентрации электролитов. Потоотделение не является основным механизмом, регулирующим содержание жидкости в организме. Следовательно, дети страдают от дефицита воды чаще, чем взрослые. Как первичная, так и вторичная гипервентиляция, связанная с метаболическим ацидозом, в значительной степени увеличивает легочную отдачу воды. Так как выдыхаемый воздух насыщен водяными парами, то в случае, если минутный объем дыхания увеличится в 5—6 раз по сравнению с нормальным, суточная потеря воды легкими у грудного ребенка может превысить 100 мл/кг. При первичной гипервентиляции наряду с экси-козом может возникнуть респираторный алкалоз. Поскольку в подобном случае процессы компенсации ведут к уменьшению содержания бикарбонатов и гиперхлоремии, то характер изменений водно-солевого обмена у больного с эксикозом и гипервентиляцией может быть ошибочно принят за ацидотическое состояние, если в распоряжении врача находятся только данные о содержании бикарбонатов. В сомнительных случаях необходимо определить значение рН, которое при первичной гипервентиляции в связи с усиленной отдачей СО2 повышено. Потери воды и солей с калом всегда надо учитывать, так как организм секретирует большое количество воды и электролитов с пищеварительными соками. Очень важен кругооборот жидкости между плазмой крови и кишечным трактом. У взрослого человека из плазмы в верхние отделы пищеварительного тракта за сутки выделяется 8 л солесодержащих жидкостей: слюны, желудочного сока, желчи, панкреатического и кишечного сока. Эти жидкости всасываются в нижних отделах кишечника, не более 100 г в день выделяется с фекалиями. У здорового ребенка в кале содержится 75—85 % воды — такое же количество, как и у взрослого. В среднем у ребенка в возрасте 2—3 мес образуется в сутки 6—30 г кала, в возрасте 6—12 мес — 10—40 г, в возрасте 1—5 лет — 15—75 г, в возрасте 6—15 лет — 70—120 г (у взрослого 100—250 г). При желудочно-кишечных расстройствах количество каловых масс и жидкости может значительно возрастать. Еще большее количество жидкости циркулирует и движется через почки: ежедневно только 1 — 1,5 л гломерулярного фильтра преобразуется в конечную (вторичную) мочу, остальная часть реабсорбируется в канальцах. Экскреция воды регулируется изменением скорости образования мочи. Снижение осмолярности плазмы указывает на чрезмерное насыщение водой, это корригируется с помощью экскреции большого объема разведенной мочи, имеющей меньшую осмолярность, чем плазма. Наоборот, когда осмолярность плазмы выше нормы, объем выделяемой мочи уменьшается, а ее осмолярность увеличивается по сравнению с осмолярностью плазмы. Вместе с тем объем мочи может быть уменьшен до количества, необходимого для растворения выводимых веществ, и поэтому зависит от диеты. Если вода не поступает в организм, то в лучшем случае в почках образуется минимальное количество максимально концентрированной мочи. У детей старше 2 мес максимальная концентрация мочи составляет 1400 мосм/л, а в возрасте менее 2 мес она достигает 700 мосм/л. На диурез влияют скорость клубочковой фильтрации, состояние эпителия почечных канальцев, концентрация в плазме надпочечниковых стероидов. Выведение мочи у грудных детей относительно массы тела больше, чем у взрослых. На выведение одного и того же количества мочевины, мочевой кислоты, креатинина, ионов затрачивается в 2—3 раза больше воды, чем у взрослых. Суточный диурез у детей старше года можно приблизительно рассчитать по формуле: 600 +100 (п-1), где п — возраст в годах. Соответственно суточная потребность детей в воде больше, чем у взрослых (табл. 98). При прекращении поступления жидкости новорожденный потерял бы полностью весь объем внеклеточной жидкости в течение 3, а взрослый — в течение 7 сут. У новорожденных и грудных детей не развито чувство жажды, этим объясняется их склонность к дегидратации. Потребность детей в воде
Система регуляции водного баланса обеспечивает два основных гомеостатических Процесса: во-первых, поддержание постоянства общего объема жидкости в организме и, во-вторых, оптимальное распределение воды между водными пространствами и секторами организма. К числу факторов поддержания водного гомеостаза относятся осмотическое и онкотическое давление жидкостей водных пространств, гидростатическое и гидродинамическое давление крови, проницаемость гистогематических барьеров и других мембран, активный транспорт электролитов и неэлектролитов, нейроэндокринные механизмы регуляции деятельности почек и других органов выделения, а также питьевое поведение и жажда. Для гомеостаза электролитов необходимо взаимодействие нескольких процессов: поступление их в организм, перераспределение и депонирование в клетках и их микроокружении, выделение из организма. Поступление электролитов в организм зависит от состава и свойств пищевых продуктов и воды, особенностей их всасывания в желудочно-кишечном тракте и состояния энтерального барьера. Однако, несмотря на широкие колебания количества и состава поступающих пищевых веществ и воды, водно-солевой баланс в здоровом организме неуклонно поддерживается за счет изменений экскреции с помощью органов выделения. Основную роль в этом гомеоста-тическом регулировании выполняют почки. То есть постоянство осмотической концентрации, ионного состава и объема жидкостей внутренней среды обеспечивается осморегулирующими, ионорегулирующими и волюморегулирующими рефлекторными механизмами. Особенно интенсивные возрастные изменения этих механизмов происходят в течение 1-го года жизни. Химическое строение пространств таково, что на нагрузки они прежде всего реагируют «сглажив'анием». Наряду с этим начинаются более сложные регуляторные процессы, направленные в сторону возможно более полного восстановления равновесия. Эти системы работают по принципу обратной связи. Автоматизм обеспечивается тем, что регуляторный характер определяется самим стимулом, приводящим систему в движение, точнее, малейшим отклонением от нормальных величин. Этот раздражитель улавливается рецепторами, которые возбуждают деятельность посредников — в большинстве случаев гормонов — в исполнительном органе, например в почечных канальцах. По устранении стимула рецептор получает об этом «сообщение» посредством обратной связи, и прекращается деятельность посредников и их синтез. По данному принципу функционирует как осмо-, так и волюморегуляция. Концентрация натрия в плазме (осмотическое давление) регулируется системой антидиуретического гормона, находящегося под управлением гипоталамических осморецепторов. Система обратной связи приводится в движение при изменении концентрации натрия, даже если отклонение от нормы невелико. Тот же стимул возбуждает гипоталамический центр жажды. Поэтому при гипернатриемии повышается потребление воды и понижается диурез; напротив, при гипонатриемии диурез повышается, ощущение жажды уменьшается и снижается потребление жидкости. Эти корригирующие процессы продолжаются до тех пор, пока не установится физиологическая концентрация натрия, о чем рецепторы получают информацию. Осморегуляция. Увеличение мочеобразования при избыточном поступлении воды у новорожденных осуществляется клу-бочковым аппаратом. В раннем возрасте мочеобразование возрастает соответственно изменению скорости клубочковой фильтрации. В раннем постнатальном онтогенезе значительную роль в регуляции водно-солевого гомеостаза играют эфферентные нервы почек. У новорожденных эфферентные нервы оказывают на почки трофическое влияние, денервация влечет за собой атрофию почки, особенно мозгового вещества. В первые месяцы после рождения нервная система регулирует величину мочеобразования, симпатические вазомоторные волокна влияют на скорость клубочковой фильтрации. Действие вазопрессина на выведение воды и натрия в онтогенезе возникает не одновременно, влияние на выведение натрия появляется позже, а это снижает эффективность осморегуляции в первые месяцы после рождения. Новорожденные значительно медленнее, чем взрослые, выводят калий при его избытке. Это обусловлено низкой секрецией калия в дистальных канальцах. Когда рефлекторное усиление выведения калия еще только появляется, оно не имеет специфического характера: усиленно выводятся ионы не только калия, но и натрия. Прием небольших доз калия детьми 10 лет сопровождается усилением выведения не только калия, но и натрия. Избирательное и эффективное выведение избытка только калия развивается лишь у подростков. У новорожденных значительно медленнее выводятся избытки ионов кальция и магния, чем у взрослых. Регуляция объема жидкости (волюморегуляция). Уменьшение количества крови, притекающей к сердцу (гиповолемия), вызывает снижение диуреза и уменьшение экскреции натрия. Увеличение объема крови (гиперволемия) приводит к противоположной реакции. Раздражение волюморецепторов правого предсердия снижает секрецию ренина и через посредство альдостерона усиливает экскрецию натрия. Раздражение рецепторов левого предсердия через супраоптическое и паравентрикулярные ядра гипоталамуса уменьшает секрецию вазопрессина. У новорожденных волюморегулирующий рефлекс, вероятно, отсутствует (опыты на животных). Способность выводить из организма избыток воды и натрия в периодах раннего и первого детства выражена слабее, чем у взрослых. Отсутствие волюморегулирующего рефлекса у маленьких детей связано с особенностями состояния ренин-ангиотензин-альдостероновой системы. Уже у плода 5 мес почки содержат ренин. Ко времени рождения концентрация ренина в плазме крови в 30 раз выше, чем у взрослых. Этим определяются высокий уровень реабсорбции натрия в дистальных сегментах нефрона. Гиперволемия в раннем возрасте не снижает секрецию ренина и альдостерона. Возможно, слабость реакции почек на гиперволемию связана также с низкой секрецией на-трийуретического фактора. Регуляция кислотно-щелочного равновесия. У новорожденных и грудных детей относительно низка концентрация бикарбонатов во внеклеточной жидкости. Почки детей не способны к достаточно эффективной реабсорбции бикарбонатов. Аммиак и, особенно, ионы водорода секретируются эпителием канальцев медленнее и в меньшем количестве, чем у взрослых. Таким образом, эффективность почек в регуляции кислотно-щелочного равновесия невысока. Это следует учитывать при питании детей коровьим молоком, приводящем к образованию кислых продуктов. СЕМИОТИКА ИЗМЕНЕНИЙ ВОДНОГО БАЛАНСА. Избыточное поступление и образование воды при неадекватно малом ее выделении из организма ведет к накоплению воды, и этот сдвиг водного баланса называется гипергидратацией. При гипергидратации вода накапливается в основном в интерстициальном водном секторе. Значительная степень гипергидратации проявляется водной интоксикацией (гипотоническая гипергидратация). При этом в интерстициальном водном секторе осмотическое давление становится ниже, чем внутри клеток, они поглощают воду, набухают, и осмотическое давление в них становится тоже сниженным. В результате повышенной чувствительности нервных клеток к уменьшению осмолярности водная пмюксикация может сопровождаться возбуждением нервных центров и мышечными судорогами. Недостаточное поступление и образование воды или чрезмерно большое ее выделение приводят к уменьшению водных пространств, главным образом интерстициального сектора, что называется дегидратацией. Это состояние сопровождается сгущением крови, ухудшением ее реологических свойств и нарушением гемодинамики. Недостаток в организме воды в объеме 20 % массы тела ведет к летальному исходу. Развитие дегидратации связано со срывом компенсации; увеличение количества теряемой воды до тех пор не приводит к эксикозу, пока поступление жидкости и немедленно вступающая в действие почечная регуляция способны поддерживать равновесие. Нарушение баланса жидкости и электролитов у детей чаще всего наблюдается при заболеваниях органов пищеварения — диарее, рвоте и характеризуется разной степенью дегидратации (табл. 99, 100). Клинические признаки дегидратации: 1. Снижение массы тела на 5 % и более. Опасная для жизни недостаточность кровообращения наступает тогда, когда потеря натрия приближается к 10—15 мэкв/кг или когда величина потери экстрацеллюлярной жидкости достигает 8—10 % от веса тела. Наиболее часто (около 75 % случаев) наблюдается изотоническая дегидратация — пропорциональная потеря воды и натрия. Осмотическое давление жидкости, теряемой через желудочно-кишечный тракт, понижено (гипотонический раствор), во внеклеточной жидкости оно остается нормальным (изотонический раствор). Происходит потеря воды из клеток. При острых желудочно-кишечных расстройствах она теряется с рвотными массами и калом. При этом происходит почти одновременное снижение содержания как воды, так и электролитов. Оценка тяжести дегидратации у детей (рекомендации ВОЗ)
Дифференциально-диагностические признаки внутриклеточного и внеклеточного обезвоживания
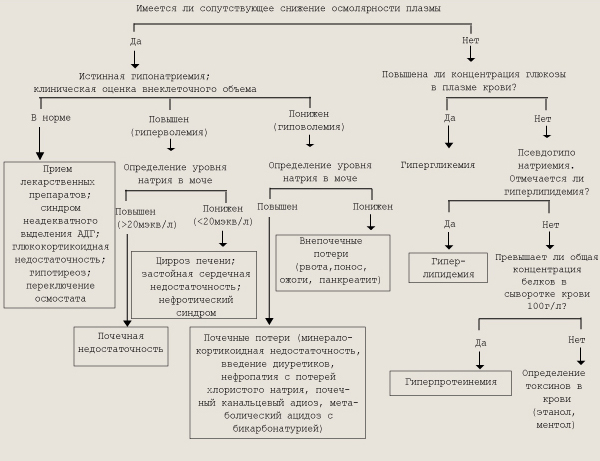
Гипертоническая дегидратация (потеря воды при избытке натрия) развивается в 25 % случаев. Вначале теряется жидкость из клеток, внеклеточная жидкость сохраняется дольше. Чистая форма этой дегидратации возможна при так называемом тепловом ударе вследствие потери жидкостей (вода и хлориды выводятся с потом). СЕМИОТИКА НАРУШЕНИЙ ОБМЕНА НЕКОТОРЫХ ИОНОВ. Нарушения ионного обмена могут быть обусловлены следующими факторами: увеличением или уменьшением количества воды в организме, уменьшением или увеличением общего количества какого-либо иона в организме. Чаще в педиатрической практике встречаются гипер- и гипонатриемия, гипер- и гипокалиемия, гипер- и гипокальциемия, гипер- и гипомагниемия, гипер- и гипохлоремия. Гипернатриемия. Концентрация натрия и содержание воды в организме могут изменяться независимо друг от друга, что приводит к гипер- или гипонатриемии. Следует подчеркнуть, что по величине концентрации натрия еще нельзя судить об общем содержании его в организме. Гипернатриемия не всегда означает избыток соли, а гипонатриемия — ее недостаток: эти изменения концентрации отражают только сдвиги в соотношении содержания воды и соли. Гипернатриемией называется состояние, при котором концентрация натрия в сыворотке крови превышает нормальные пределы (145—150 мэкв/л). Общим признаком гипернатриемии является клеточный эксикоз, вследствие повышения экстрацеллюлярной осмотической концентрации происходит выход воды из клеток. Количество экстрацеллюлярной жидкости может быть понижено при гипернатриемии с тотальным эксикозом и повышено при гипертоническом увеличении объема экстрацеллюлярной жидкости. Гипернатриемия может возникать при уменьшении общего количества воды в организме и неизмененном количестве натрия или при потерях жидкости, более гипотоничной по сравне- нию с сывороткой крови. Это происходит вследствие недостаточного поступления воды, например при лихорадке или в результате потерь жидкости при повышенном потоотделении, несахарном диабете. Такое состояние соответствует гипертонической дегидратации. При диарее, несмотря на гипернатриемию, имеет место дефицит натрия; только при потере соли, превышающей потери воды, развивается гипонатриемия. Гипернатриемия может быть вызвана увеличением общего количества натрия в организме. Причины увеличения общего содержания натрия различны, но основная — превышение поступления над выведением. Это происходит прежде всего при ограничении выделительной функции почек (острая и хроническая почечная недостаточность). Причиной гипернатриемии может быть передозировка хлорида или бикарбоната натрия при инфузионной терапии, повышение уровня альдостерона в крови (увеличение реабсорбции ионов натрия в канальцах почек), усиленная секреция глюкокортикоидов, например в первые дни постагрессивного периода (задержка натрия в организме). Могут отмечаться возбуждение, лихорадка, сильная жажда, сухость слизистых оболочек. В тяжелых случаях в клинической картине доминируют церебральные симптомы — судороги, нарушение сознания. При гипертонической гипсргидратации отмечаются отеки. При хронической гипернатриемии может отмечаться отставание в умственном развитии. Считается, что причиной церебральных нарушений являются повреждающие осмотические факторы, дегидратация клеток; в тяжелых случаях могут произойти кровоизлияния в мозговые оболочки или вещество мозга — гипернатриемическая геморрагическая энцефалопатия, которая развивается в результате особенно остро наступившей гипернатриемии. Гипонатриемия констатируется при концентрации натрия в плазме ниже 135 мэкв/л. Основой ее развития являются отрицательный баланс натрия или положительный баланс воды. Выделяются три основных типа гипонатриемии: 1) обусловленная дефицитом соли, Дефицит натрия вызывают экстраренальные потери — рвота, понос, сильное потоотделение (особенно у лихорадящих детей с муковисцидозом); уменьшенное потребление поваренной соли при бессолевой диете, отсутствии аппетита. Ренальные потери натрия возникают при хроническом гломе-руло- и пиелонефрите, при уремии с полиурией, терапии салу-ретиками. Диагностический поиск при гипонатриемии представлен на рис.
Диагностический поиск при синдроме гипонатриемии У новорожденных потери натрия наблюдаются вследствие незрелости ренин-ангиотензин-альдостероновой системы или сниженной реакции почечных канальцев на альдостерон. Гипо-натриемия является одним из признаков нефротического синдрома, адреногенитального синдрома с потерей солей и синдрома Уотерхауса -Фридериксена. Острая гипонатриемия разведения (гипотоническая гипергидратация — водная интоксикация) в большинстве случаев имеет ятрогенное происхождение, развивается при несоответствующем поступлении в организм натрия и воды. Ее причинами являются введение чрезмерно больших количеств гипотонического раствора при эксикозе, шоке или послеоперационном состоянии, бесконтрольное применение диуретиков при таких отечных состояниях, когда процессы ретенции воды преобладают над регуляцией ионного равновесия; перегрузка жидкостью больных с анурией. В основе патофизиологических нарушений лежит гипотонический отек клеток. Его признаками являются головная боль, рвота, подергивания икроножных мышц, общие судороги. Гипокшшемия. Дефицит калия наблюдается при отрицательном балансе иона, то есть нарушении равновесия между поступлением иона с пищей и его выделением. Увеличению выведения калия из организма способствует катаболическая направленность метаболизма, при которой происходят активный распад клеточного белка и снижение выработки энергии клетками, что способствует выходу калия из клетки даже при неповрежденной мембране. Клинические состояния, при которых наиболее часто встречается гипокалиемия
Повышенные потери калия могут быть вызваны рядом причин: 1) большими желудочно-кишечными потерями калия при продолжительной рвоте, поносе, хроническом истечении желудочно-кишечной жидкости из фистулы; Вследствие дефицита калия поражаются все мышцы: поперечнополосатые, гладкие и сердечная мышца, а также почки. Эти изменения обусловливают патофизиологические реакции и определяют основную клиническую симптоматику — выраженную мышечную слабость, параличи, отсутствие рефлексов; метеоризм, запоры, паралитический илеус; изменения ЭКГ (снижение вольтажа зубца R, удлинение интервала Q— Т, уплощение зубца Т и смещение сегмента ST от изоэлектрической линии), признаки миокардита, дилатацию сердца, повышенную чувствительность к дигиталису, остановку сердца; нарушения процесса дыхания (отчасти связаны с метеоризмом), паралич дыхательной мускулатуры до развития асфиксии; нефропатию с полиурией, гипостенурией, паралич мочевого пузыря. Так как калий является структурным элементом клеток, то его недостаток проявляется нарушением физического развития. Страдающие от дефицита калия больные, до того как недостаток калия распознан, часто впервые обращаются к невропатологам, гастроэнтерологам или нефрологам с жалобами на мышечную слабость, метеоризм или полиурию. Острый дефицит калия часто присоединяется к тяжелым состояниям, особенно к эксикозу, выраженные симптомы которого маскируют менее выраженные клинические признаки калиевой недостаточности. Концентрация сывороточного калия малоинформативна, так как 98 % калия находится внутриклеточно. Несмотря на недостаток калия в клетках, его концентрация в крови может быть высокой или нормальной (при стрессе, олигурии или ацидозе). Часто дефицит калия обнаруживается только после устранения этих состояний, например после ликвидации ацидоза, когда калий из обедненного внеклеточного депо поступает в клетки, также страдающие от дефицита. Диагноз дефицита калия наиболее объективно подтверждается ею внутриклеточным уровнем, что в клинической практике соответствует анализу концентрации К+ в эритроцитах. Наиболее существенное значение для функции клетки имеют не абсолютные значения концентрации К+ внутри- и внеклеточно, а их соотношение (в норме 1:20 — 1:30). При концентрации калия в сыворотке крови ниже 3,5 мэкв/л можно говорить о гипокалиемии, дальнейшее снижение уровня калия — ниже 2,5 мэкв — является очень серьезным (в тяжелых случаях концентрация калия в плазме может упасть до 1,2 мэкв/л). На ЭКГ при гипокалиемии наблюдаются плоские или инвертированные зубцы Т, удлинение интервала Q— Т, увеличение систолического показателя, снижение сегмента ST, удлинение интервала Р—Q, нарушения ритма и проводимости. Гиперкалиемия — повышение концентрации калия в сыворотке крови свыше 5,8—6 ммоль/л у взрослых и детей старше 1 мес жизни и более 6—7 ммоль/л у новорожденных. Причины гипер-калиемии следующие: значительное или полное прекращение выделения К+ с мочой, наблюдаемое при почечной недостаточности, которая обусловлена преренальными и ренальньши причинами, сольтеряющая форма адреногенитального синдрома, недостаточность коры надпочечников (табл. 102). Гиперкалиемия сопутствует повышенному распаду клеток, особенно при гемолизе, при быстром введении больших доз калия внутривенно без соответствующего энергетического обеспечения или введении раствора калия на фоне сниженной функции почек. Причины гиперкалиемии
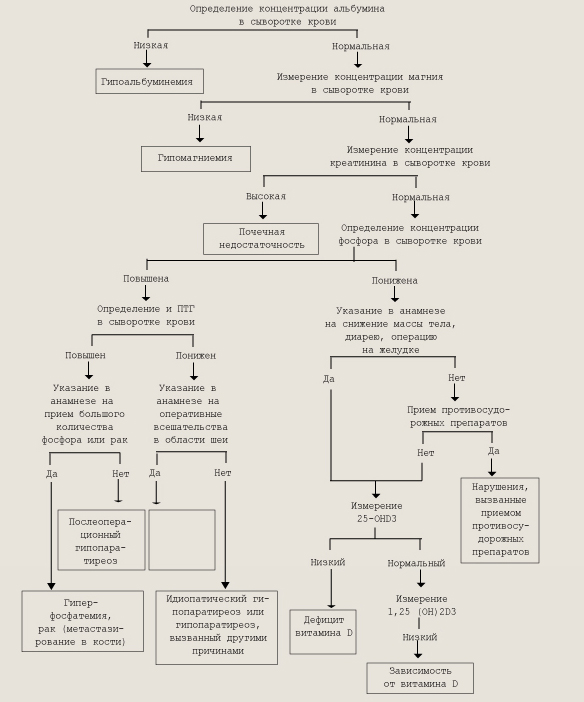
Гиперкалиемия проявляется адинамией, вялыми параличами мышц, характерна брадикардия, снижается артериальное давление. При прогрессировании гиперкалиемии происходит остановка сердца в диастолу. Наиболее ранними являются ЭКГ-признаки: уменьшение ЧСС, нарушение ритма, расширение комплекса QRS, высокий заостренный зубец Т, блокада ножек пучка Гиса, удлинение интервала Р— Q. Гипокальциемия — снижение содержания ионов кальция в сыворотке крови ниже 2 ммоль/л, которое может быть связано с недостаточным поступлением кальция с пищей, нарушением его всасывания в кишечнике (синдром мальабсорбции, тяжелая диарея), увеличенным выделением кальция при жидком стуле, наличии свищей и дренирования тонкой кишки. Нарушения обмена кальция характерны для хронических заболеваний почек (гипокальциемическая форма витамин-О-независимого рахита, хроническая почечная недостаточность с почечной остеодист-рофией, нефротический синдром) и эндокринных желез (гипопаратиреоз, псевдогипопаратиреоз, синдром Ди Георге). Гипокаль-циемия наблюдается также при нарушении метаболизма витамина D, рахите, после переливания больших количеств крови, при резком увеличении концентрации белка в сыворотке крови. Гипокальциемия проявляется следующими характерными признаками: клинические симптомы скрытой (симптомы Хвос-тека, Люста, Эрба, Маслова и др.) или манифестной (ларин-госпазм, карпопедальный спазм, эклампсия) спазмофилии в сочетании с типичными изменениями ЭКГ — удлинением интервала Q— Т за счет сегмента ST без расширения зубца Т. Диагностический подход при гипокальциемии приведен на рис. Гиперкальциемия — увеличение содержания кальция в сыворотке крови более 3 ммоль/л. Уровень кальция может повышаться при нарушении выведения кальция или при значительном его поступлении в организм. Повышение уровня кальция наблюдается при гиперпаратиреозе, иммобилизационном остеопорозе, гипофосфатазии, хронической идиоп этической гиперкальциемии. Гиперкальциемия наблюдается также при злокачественных заболеваниях с поражением скелета, в том числе при остром лейкозе, интоксикации витамином D. Клинически Гиперкальциемия проявляется тошнотой, частой рвотой, адинамией и жаждой. Типичные изменения на ЭКГ: укорочение интервала Q— Т за счет сегмента ST. Гипомагниемия — снижение уровня магния в сыворотке крови ниже 0,5—0,65 ммоль/л. Гипомагниемия наблюдается при синдроме мальабсорбции, недостаточном питании, гипопаратире-озе, циррозе печени, лечении диуретиками, гиперкальциемии, почечном канальцевом ацидозе, первичном альдостеронизме. Первоначальные признаки гипомагниемии — повышенная нервно-мышечная возбудимость (скрытая или явная тетания, изнуряющие судороги и тремор, которые не купируются внутривенным введением препаратов кальция, витамина D2 и парат-гормона), анорексия, изменения сердечного ритма и ЭКГ. Гипермагниемия — увеличение концентрации магния в сыворотке крови более 2,5 ммоль/л. Наблюдается при нарушении функции почек, после применения магнийсодержащих слабительных, клизм и жидкости для внутривенного введения. Клинически гипермагниемия проявляется гипорефлексией, которая предшествует угнетению дыхания, сонливости и коме, при высоких концентрациях может наступить остановка сердца. Гипохлоремия — снижение концентрации хлора в сыворотке крови ниже 100—95 ммоль/л. Нарушение обмена хлора происходит одновременно с нарушениями обмена натрия и калия. Гипохлоремия возникает при нефизиологических потерях из ЖКТ (рвота, желудочный дренаж, обильное промывание желудка водой и др.).
Диагностический поиск при синдроме гипокальциемии Клиническая картина гипохлоремии неспецифична, однако при более значительных потерях хлора по сравнению с потерями натрия (потеря соляной кислоты) может развиться гипохло-ремический алкалоз. Гиперхлоремия — увеличение концентрации иона хлора в сыворотке крови более 115—120 ммоль/л. Повышение концентрации хлора в сыворотке обычно происходит одновременно с повышением уровня натрия и обусловлено большим поступлением иона в организм при уменьшении выделения его с мочой. Клиническая картина неспецифична, может наблюдаться гипер-хлоремический ацидоз. Поделитесь этой записью или добавьте в закладки |
 Главная
Главная